中科院陈雁研究组揭示肝脏脂肪酸代谢关键调控机制
中科院陈雁研究组揭示肝脏脂肪酸代谢关键调控机制
1月13日,国际知名学术期刊Hepatology在线发表了中国科学院上海生命科学研究院(人口健康领域)陈雁研究组的最新研究成果“Hepatic PPARα function is controlled by polyubiquitination and proteasome-mediated degradation via the coordinated actions of PAQR3 and HUWE1”。该研究揭示了孕酮和脂联素受体3(PAQR3)通过促进PPARα泛素化及蛋白酶体途径依赖的降解进而调控肝脏脂质代谢的作用机制。
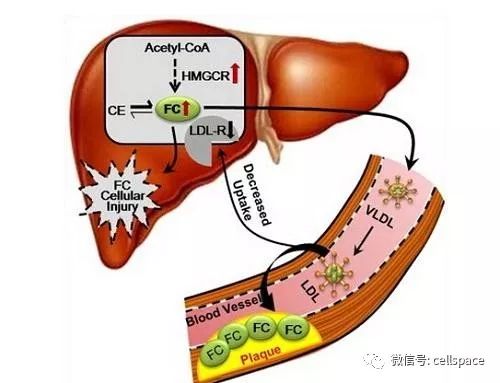
过氧化物酶体增殖物激活受体α(PPARα)是一个重要的核受体,在维持机体能量代谢稳态方面发挥着重要作用。当机体处于营养缺乏状态,包浆中的PPARα会转移到细胞核中,入核的PPARα会促进下游参与脂肪酸氧化相关基因的表达从而促进脂肪酸氧化以保证机体正常的能量需求并维持肝脏脂代谢稳态。脂肪酸氧化是肝脏脂代谢的主要通路之一,如果肝脏中积累的脂质不能及时代谢清除将会引起肝脏中脂质积累,严重时会引发肝脏脂肪变性进而导致非酒精性脂肪肝。曾有研究表明,高脂饮食会诱发PPARα肝脏特异性敲除的小鼠发生严重的脂肪肝,但是PPARα的翻译后修饰如何调控肝脏脂代谢的机制目前尚不清楚。
在陈雁研究员的指导下,博士研究生赵子龙等发现,利用腺病毒干扰技术,在小鼠肝脏中PAQR3能够影响长时间禁食导致的肝脏内甘油三酯的积累。通过构建肝脏特异性PAQR3敲除的小鼠发现,PAQR3敲除的小鼠可以缓解长时间禁食导致的脂肪肝形成。通过一系列的生化及细胞实验,研究人员发现PAQR3可以影响PPARα的蛋白水平但不改变其mRNA水平,深入的分析揭示PAQR3可以促进PPARα蛋白的泛素化从而影响PPARα的半衰期,进一步的研究发现参与PPARα降解的E3泛素连接酶HUWE1。
该研究为深入了解肝脏脂质稳态平衡中的分子机制提供了新的理论基础,同时表明,深入探讨PAQR3-HUWE1-PPARα这一信号通路,将为治疗非酒精性脂肪肝等代谢性疾病提供新的治疗靶点及思路。
该研究得到了华东师范大学廖鲁剑教授的大力支持和帮助。该课题得到国家自然科学基金,科技部973基金以及中科院等经费的支持。(科技处)